多地首方
PSORIASIS NEWS
中国医学科学院皮肤病医院开出首张替瑞奇珠单抗注射液处方
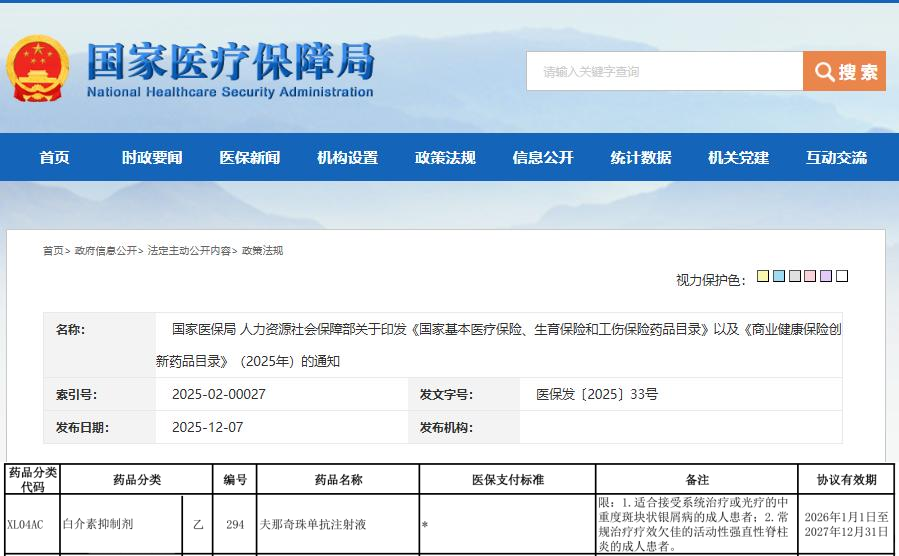
纳入医保
2023年5月26日,益路取(替瑞奇珠单抗注射液)获中国国家药品监督管理局批准上市,用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者。12月13日,《国家基本医疗保险、工伤保险和生育保险药品目录(2023年)》发布,益路取成功获纳入国家医保目录乙类范围,进一步提升其可及性和可负担性。
产品特点
靶点明确,精准打击
替瑞奇珠单抗是一种人源化的lgG1/κ单抗,旨在选择性地与白细胞介素-23(IL-23)的p19亚基结合,并抑制其与IL-23受体相互作用,从而抑制促炎症细胞因子和趋化因子的释放,减轻银屑病的皮损严重程度1。
持续应答,远期长效
中国III期临床试验及全球扩展性研究结果显示1,4,替瑞奇珠单抗的主要疗效评估指标PASI 75应答率随治疗时间的推移持续上升。替瑞奇珠单抗治疗28周可达到高水平应答,1年PASI 75应答率维持在91.3%,5年PASI 75应答率高达93.9%,远期疗效十分优异。
注射数少,依从性高
替瑞奇珠单抗的注射次数极少1,首月2针,维持期一年仅需给药4针,治疗便利,可以带来更高的患者依从性。
安全耐受,易于管理
替瑞奇珠单抗长期应用的安全性和耐受性良好,总体AE发生率与安慰剂组相当1,且均为临床常见不良反应,最常见不良反应为鼻咽炎。5年随访数据显示,因不良反应停药比例<1%2。
一项已发表的荟萃分析显示,益路取发生不良事件和严重不良事件的风险均为最低3。
权威指南,一致推荐
作为当前银屑病领域的热点生物制剂,替瑞奇珠单抗注射液在中国、美国、欧洲、英国等全球多个国家都获得了临床诊疗指南的一线推荐5-10。
益路取(替瑞奇珠单抗注射液)
作为一家把控产品全生命周期管理的开放式平台型企业,康哲药业将积极开展银屑病相关的学术交流活动,快速实现益路取的全渠道商业化覆盖。“路遥知马力,益取价更优”,益路取(替瑞奇珠单抗注射液)将为广大中国银屑病患者提供安全有效、治疗便利、经济实惠、长期获益的治疗选择。
END
[1]替瑞奇珠单抗注射液说明书(批准版)
[2]Reich K, Papp KA, Blauvelt A, Tyring SK, Sinclair R, Thaçi D, Nograles K, MehtaA, Cichanowitz N, Li Q, Liu K, La Rosa C, Green S, Kimball AB. Tildrakizumab versus placebo or etanercept for chronic plaque psoriasis (reSURFACE 1 and reSURFACE 2): results from two randomised controlled, phase 3 trials. Lancet. 2017 Jul 15;390(10091):276-288. doi: 10.1016/S0140-6736(17)31279-5.
[3]Bai F, Li GG, Liu Q, Niu X, Li R, Ma H. Short-Term Efficacy and Safety of IL-17, IL-12/23, and IL-23 Inhibitors Brodalumab, Secukinumab, Ixekizumab, Ustekinumab, Guselkumab, Tildrakizumab, and Risankizumab for the Treatment of Moderate toSevere Plaque Psoriasis: A Systematic Review and Network Meta-Analysis of Randomized Controlled Trials. J Immunol Res. 2019 Sep 10;2019:2546161. doi: 10.1155/2019/2546161.
[4]P011临床试验(替瑞奇珠单抗全球关键III期试验)报告
[5]1.中华医学会皮肤性病学分会,中国银屑病诊疗指南(2023版).
[6]2. Menter A, et al. J Am Acad Dermatol. 2019 Apr;80(4):1029-1072.
[7]3. Nast A, et al. J Eur Acad Dermatol Venereol. 2020 Nov;34(11):2461-2498.
[8]4. Smith C, et al. Br J Dermatol. 2020 Oct;183(4):628-637.
[9]5. Podoswa-Ozerkovsky N, et al. Gac Med Mex. 2020;156(5):446-453.
[10]6. Nast A, et al. Dtsch Dermatol Ges. 2021;19(6):934-150.








Leave a Reply