两项大型调查研究表明,57%接受传统药物治疗的患者和45%接受生物制剂治疗的患者都存在停药问题,究其原因,主要在于药物安全性、耐受性、有效性不足,及治疗过程中的监测负担和药物注射等问题[3,4]。此外,报告中也指出,43%的银屑病患者饱受瘙痒症状的困扰[3]。因此,广大银屑病患者亟需有效、安全、便捷且能有效改善瘙痒症状的新型治疗方法。
2022年7月21日,由复星医药主办的“化繁为简,由口皆碑——阿普米司特片专家顾问会”正式召开,大会邀请多位银屑病领域权威专家在此学术交流、碰撞火花,拓宽中国银屑病诊疗的新思路和新理念。

大会开始之前,复星医药国内营销平台CEO袁春先生表示,2022年6月复星医药与安进宣布就创新药物欧泰乐(阿普米司特片)达成合作。此次合作将使安进借助复星医药在中国的商业能力,以更快的速度惠及中国的银屑病患者。
这是国内第一场阿普米司特的AB会,郑重感谢各位银屑病领域大咖对会议的大力支持。复星医药一直致力于银屑病患者的全程管理,利用自身国际化优势,从生物制剂到小分子药物,为银屑病患者提供了全面的药物保障和一体化的诊疗方案。这与各位医生们希望造福更多患者的目标一致,期待接下来的这一场学术盛宴。
本次大会特邀复旦大学附属华山医院皮肤病研究所的张学军教授和中国医科大学附属第一医院的高兴华教授担任大会主席。



本场会议由张学军教授担任主持,北京大学第三医院的张春雷教授带来题为《银屑病治疗新通路:PDE4抑制剂——阿普米司特》的专题演讲。张春雷教授从作用机制、临床数据和患者需求三方面分享了阿普米司特开拓银屑病治疗新通路的局面。
磷酸二酯酶4(PDE4)是环磷酸腺苷(cAMP)特异性水解酶,表达于多种炎性细胞,是炎性细胞中主要的PDE。阿普米司特抑制剂特异性抑制PDE4,通过cAMP调节促炎因子及抗炎因子平衡,从而抑制多种银屑病相关炎症细胞因子,如IL-17F,IL-17A,IL-22和TNF-α[5,6]。
循证医学数据显示,在中重度斑块状银屑病患者中,阿普米司特应答迅速。与安慰剂组相比,第2-4周针对银屑病面积和严重程度指数(PASI)的应答率已出现曲线分离,并持续改善[7,8]。ESTEEM 1 研究结果显示,持续接受阿普米司特治疗52周,PASI评分较基线改善保持稳定(81%-88%),这些受试者中约 61% 在第52周时达到 PASI-75 应答[7];ESTEEM 2 研究结果显示,持续接受阿普米司特治疗的61例患者,80%在第52周出现PASI-50应答[8]。
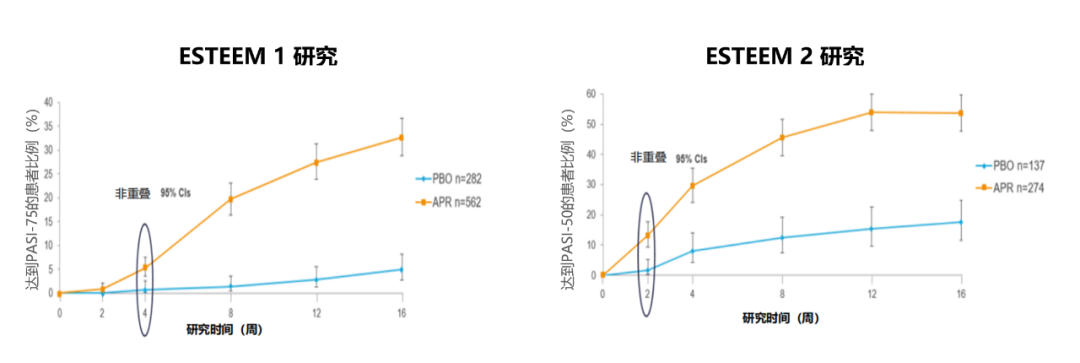
图:ESTEEM 1&2研究PASI-75、PASI-50结果
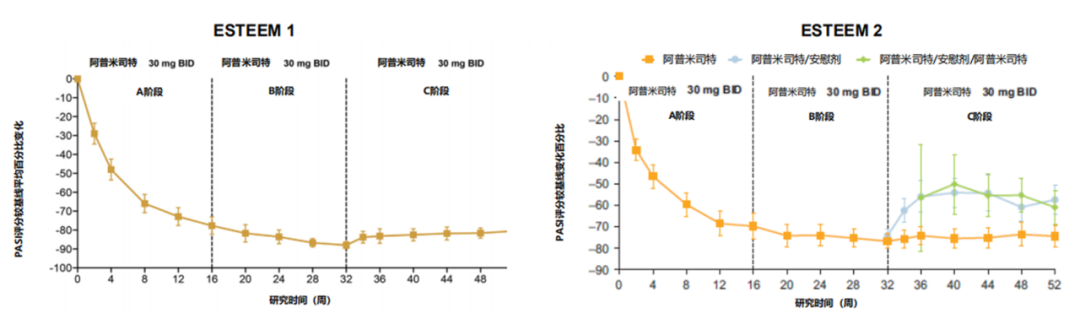
此外,阿普米司特可显著改善甲银屑病和头皮银屑病患者的临床症状[7-9]。同时,安全性数据显示,阿普米司特随访3年,没有报告严重的机会性感染、结核复发。可见,阿普米司特快速长效,可以改善银屑病患者生活,且长期安全性高,耐受良好。
对于银屑病患者而言,阿普米司特治疗依从性高,药物维持率达85.3%,严重不良事件(SAE)发生率低,仅6.3%的患者因治疗相关不良事件停药,有助于长期维持疗效[10]。
阿普米司特作为PDE4抑制剂口服小分子药物,是全球首款获批治疗银屑病的靶向口服药,也是被引进中国的第一批临床急需境外新药。其用药前无需进行用药筛查,疗效好,安全性高,于2021年被美国食品药品监督管理局(FDA)批准用于轻中度银屑病治疗,目前在我国的适应症是治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。因此,可以说阿普米司特在我国的获批上市,为银屑病的治疗开辟了新的道路。



本场会议由高兴华教授担任主持,由安徽医科大学第一附属医院的孙良丹教授带来题为《阿普米司特与银屑病共病治疗》的专题演讲。
孙良丹教授强调,银屑病可引起全身多种合并症出现[11],其中代谢综合征及心血管方面合并症需要重点关注。有相关研究显示,银屑病患病越久,出现银屑病关节炎(PsA)累积百分比越高[12]。
中国数据显示,我国银屑病患者的共病主要以三高、心血管疾病、代谢综合征以及抑郁症为主[13,14]。随后,孙良丹教授解读多项权威指南,分析银屑病共病的管理。其中,2019年AAD-NPF指南推荐针对患者心血管疾病、代谢综合征进行筛查,关注患者心理及生活方式[15],2020欧洲共病专家共识推荐阿普米司特用于多种合并症的银屑病治疗[16]。循证医学数据显示,阿普米司特在肥胖合并银屑病治疗有效,可改善胰岛素抵抗、代谢状态和心功能,且从病例报道及临床研究表明,阿普米司特治疗其他共病方面有应用潜力[17-20]。




来源:医学界皮肤频道





Leave a Reply